Mostrando entradas con la etiqueta 2º Bach. Mostrar todas las entradas
Mostrando entradas con la etiqueta 2º Bach. Mostrar todas las entradas
martes, 4 de febrero de 2020
Tabla periódica interactiva
Os dejo por aquí una tabla periódica interactiva, ideal para enseñar en clase e ir descubriendo los diferentes elementos.
viernes, 4 de mayo de 2018
¿Por qué estallan los Peta Z cuando los metes en la boca?
Desde que era pequeña siempre me han llamado la atención los Peta Zetas ¿te acuerdas de ellos? ¡Esa "chuche" que saltaba cuando entraba en contacto con nuestra boca!
¿Qué procesos químicos llevan a esa sensación tan absurdamente placentera? Los Peta Zetas eran la típica golosina que abrazabas con pasión durante una época pero acababa cansando. Desde luego no había ninguna otra como ella. Unas piedrecitas de colores que se meten en la boca y empiezan a hacer ¡pop! y golpeaban y rebotaban antes de romperse creando un ruido crepitante que sería alarmante si viniera de cualquier otro producto alimenticio.
Y todo dentro de tu boca, que no sabías si de aquella ibas a volver a saborear algo o esa pequeña tortura china te iba a quemar la lengua para siempre... Cuando alguno estallaba más fuerte incluso pensabas que podía atravesarte el paladar, pero no. Era bastante seguro así que volvías a comprarte otro sobre :D...
La idea surgió del científico William A. Mitchell desde EEUU, la idea fue conocida allí como Pop Rocks y empezó a venderse en 1975. Para ello encontró la clave en el dióxido de carbono; su idea era cocinar el CO2 dentro de caramelos, y aunque su experimento no despegó sentó las bases para el secreto de los Peta Zetas.
Estas piedras de colores se preparan mezclando azúcar, lactosa, saborizantes y aromatizantes. Una vez que estos ingredientes se funden, se hierven a 149ºC hasta formar un jarabe de azúcares muy espeso que pasa a un reactor que gasifica el jarabe con CO2 a una presión de 60 atm. (más o menos la misma presión que aguantaría una persona a 600 metros de profundidad).
Este proceso consigue que se formen burbujas muy pequeñas dentro del líquido. Posteriormente se enfría hasta que deja de ser un líquido denso, obteniéndose una gran masa de caramelo duro con burbujas atrapadas que ejercen una presión al sólido mayor que la que tiene una botella de champán.
La presión en el interior del caramelo es mayor que la presión exterior, por ello, la masa se rompe en pedacitos (que son las piezas irregulares que conocemos como Peta Zetas).
Al meterlos en la boca, la saliva disuelve el caramelo que envuelve a las burbujas que se liberan estallando como pequeños petardos generando los típicos ruidos y microexplosiones que conocemos.
No se conoce que un Peta Zeta haya provocado heridos, incluso si se mezcla con Coca Cola o Gaseosa (un mito que se ha perpetuado mucho en EEUU).
Y ya no solo como chuches, ¡ahora también se está utilizando en la cocina de vanguardia para la innovación! Está claro que después de esto hoy me tomaré unos Peta Zetas :D ...
miércoles, 4 de abril de 2018
Los experimentos más bellos de la historia
Se que llevo unos meses sin aparecer por aquí; pero hay que decir que ahora estoy dedicando más tiempo a estudiar que a otra cosa, pero no podía dejar de compartir este vídeo con vosotros. Prometo dar señales de vida con más asiduidad...
¿Quieres conocer cuales son los experimentos más bellos de la historia?
¡Pues toma nota porque hay alguno que está genial!
martes, 28 de noviembre de 2017
¿Cómo funciona el catalizador en un vehículo?
Muchas veces habréis escuchado la palabra catalizador en clase.
Pero sabríais explicar ¿qué es claramente y en dónde se usan habitualmente?
Pues muy atento que en dos minutos te lo explico para que no se te olvide nunca más.
En química, un catalizador es una sustancia que modifica la velocidad de una reacción sin reaccionar en esta misma. Podemos encontrar catalizadores que aumentan la velocidad de la reacción (catalizadores positivos) o en cambio, catalizadores que ocasionan una disminución de la velocidad de la misma (catalizadores negativos).
Querer que una reacción vaya más rápido, puede considerarse normal, a fin y al cabo, cualquier industria querrá reducir su tiempo de reacción, poder así producir más y obtener grandes ganancias.
Pero te puede llamar la atención para qué se necesitará por ejemplo que una reacción vaya más lenta. Pues es de gran importancia, especialmente en la industria alimentaria, ya que al existir alimentos perecederos por ejemplo, nos puede interesar ralentizar una reacción de descomposición de los mismos y poder preservarlos así por más tiempo. Seguro que has oido de los famosos "conservantes". Pues bien, estos se usan para así poder producir alimentos más seguros para el consumidor, consiguiendo prevenir la aparición de agentes biológicos.
Los conservantes consiguen inhibir, retardar o detener los procesos de fermentación, enmohecimiento, putrefacción, etc... de los diferentes alimentos.
Por eso cuando tomas un yogurt por ejemplo verás que se ha añadido sorbato de sodio, o en el vino dióxido de azufre, en la leche ácido sorbido, etc...
Pero ¿qué ocurre con el catalizador de un vehículo? ¿Sabes qué función tienen y dónde se encuentran? ¿Sabías que los metales de los que está formado cuestan más de 37000 € el kg? Quédate con la combinación de Platino (Pt) - Rodio (Rh) y Platino (Pt) - Vanadio (V) ya que unidos tienen la gran propiedad de hacer reaccionar los gases tóxicos, volver a combinarlos y crear gases inocuos para la salud.
Si el catalizador no está caliente (cercano a los 750ºC) no sirve de nada, es por ello que en distancias cortas, cuando se recorren menos de 10 km, el coche expulsa gases no tratados.
En el siguiente vídeo podemos ver toda la explicación. ¡Parece increíble ¿verdad?
¡Mucho ojo con las distancias cortas! Ahora tienes una razón más para que se fomente el uso del transporte urbano...
miércoles, 27 de septiembre de 2017
La noche de los investigadores 2017 Santander
¡Hoy os traigo un plan para este próximo viernes día 29 de Septiembre! Y esque vuelve la Noche Europea de los Investigadores organizada por la Universidad de Cantabria (UC), la cual reunirá a más de 250 científicos que mostrarán la otra cara de la ciencia y desmontarán mitos a través de 21 talleres, charlas y monólogos.
La cita será a lo largo del día 29 de Septiembre en diferentes puntos de Santander y de forma simultánea en 300 ciudades europeas; por lo que si no estás por Santander no dudes en consultar porque seguro que podrás también disfrutar de talleres muy interesantes.
En concreto en Santander, la Plaza Porticada, el Instituto de Investigación de Valdecilla o el Paraninfo de la Universidad, serán lugares de encuentro, aunque otros, como por ejemplo el taller de matemáticas, recorrerán las calles de Santander explicando los números que esconden los edificios de la ciudad.
Algunas de las actividades y de los talleres requieren de una inscripción previa vía online. Os dejo a continuación el enlace donde puedes apuntarte:
Así de divertido fue el año pasado:
Echando un vistazo, todavía quedan plazas para talleres tan interesantes como ¿por qué cambian los metales? dirigido a público de entre 9 y 16 años.
Además desde las 17 horas, el patio del colegio Numancia, albergará la tradicional Gimkana: Juega con la ciencia, organizada por el Instituto de Física de Cantabria (IFCA) y que está dirigido a niños de entre 5 y 10 años. Habrá protones, telescopios, el sistema solar, cohetes... un montón de experimentos para "tocar" la ciencia.
También destaca la actividad "Dialoga con la ciencia, dialoga con un científico", que tendrá lugar en la Plaza Porticada de 20 a 22 de la noche, allí, todo el que quiera pueda mantener una conversación de lo más interesante y conocer un poquito más de primera mano a qué se dedican en su trabajo.
¿No me digas que no estás deseando que llegue el viernes?
lunes, 18 de septiembre de 2017
Validation: Un corto que te hará sonreír
Hoy me salgo un poco de la ciencia, para traeros un corto que no puede faltar en cualquier clase de tutoría.
Conseguirá arrancar una sonrisa sin lugar a dudas a cualquiera que lo vea.
Hoy en día, con las prisas a veces nos olvidamos hasta de sonreír. Gruñidos, malas caras, contestaciones poco profesionales...etc
Por ello hoy no quería dejar pasar la oportunidad y enseñaros un cortometraje que me ha gustado de principio a fin y creo que puede llegar al corazoncito de los alumnos.
¿Quieres conocer el verdadero valor de una sonrisa? ¿Quieres conocer los beneficios de sonreir? ¿Quieres arrancar la mejor de las sonrisas entre tus alumnos?
Pues muy atentos a este corto de Kurt Kuenne que desde 2007 nos lleva enseñando que una simple sonrisa o un comentario agradable hacia otra persona es capaz de cambiarlo todo.
En su momento fue una revelación consiguiendo un gran reconocimiento y repercusión internacional. Y después de verlo puedo decir que se por qué fue así.
No me enrollo más y aquí lo tenéis. ¡Recuerda que me puedes indicar qué te ha parecido en los comentarios :D!
domingo, 17 de septiembre de 2017
Periodic Videos:¡Un canal del que se puede aprender un montón!
Ahora que se ha puesto de moda tener un canal de Youtube...He empezado a navegar y me topado con uno que me ha cautivado: Periodic Videos
Un canal exclusivo de química, rozando el millón de suscriptores y con vídeos periódicos centrados especialmente en las propiedades de cada elemento de la tabla periódica.
Son vídeos didácticos, cortitos y en inglés, con lo cual podemos matar dos pájaros de un tiro si encima vemos alguno.
Investigando un poco he podido comprobar quienes son los artífices de este canal. Y no son ni más ni menos que el departamento de química de la Universidad de Nottinghan. Un equipo formado por diez químicos que sin lugar a dudas tienen muchas curiosidades que contarnos.
En su página web (Periodic Videos) tienen una tabla periódica y pinchando en cada elemento te abre el vídeo respectivo. Porque sí es verdad que muchas veces estudiamos la tabla periódica de memoria, sin atender a los usos de los principales elementos con lo que al final resulta algo aburrido y monótono.
Creo que esta puede ser una gran opción para hacer un poquito más amenas las clases. Intercalando algún vídeo, que no duran más de 10 minutos con las explicaciones habituales.
Por lo pronto me quedo suscrita al canal y enseguida iré poniendo alguna entrada de alguna curiosidad que me guste de los vídeos.
Estas opciones deberían ser los nuevos influencers!
Vídeos que aportan, que enseñan, que crean curiosidad, etc... A más de un profesor creo que le podrían dar mucho juego.
jueves, 10 de agosto de 2017
Esto ocurre cuando se ingiere alcohol
Uno de los protagonistas los fines de semana de muchos jóvenes es el alcohol. La principal bebida alcohólica que se consume es la querida cerveza, y más ahora que con el buen tiempo apetece beberse una bien fresquita.
Las bebidas que más se consumen durante una fiesta son las bebidas alcohólicas destiladas (ron, vodka, ginebra, etc...) que son las que más problemas causan cuando su consumo supera un límite.
El alcohol es una droga depresora del Sistema Nervioso Central que inhibe progresivamente las funciones cerebrales.
Se caracteriza por la aparición de síntomas de intoxicación que afectan a la actividad cerebral, genera falta de coordinación motora y produce cambios de comportamiento.
Se caracteriza por la aparición de síntomas de intoxicación que afectan a la actividad cerebral, genera falta de coordinación motora y produce cambios de comportamiento.
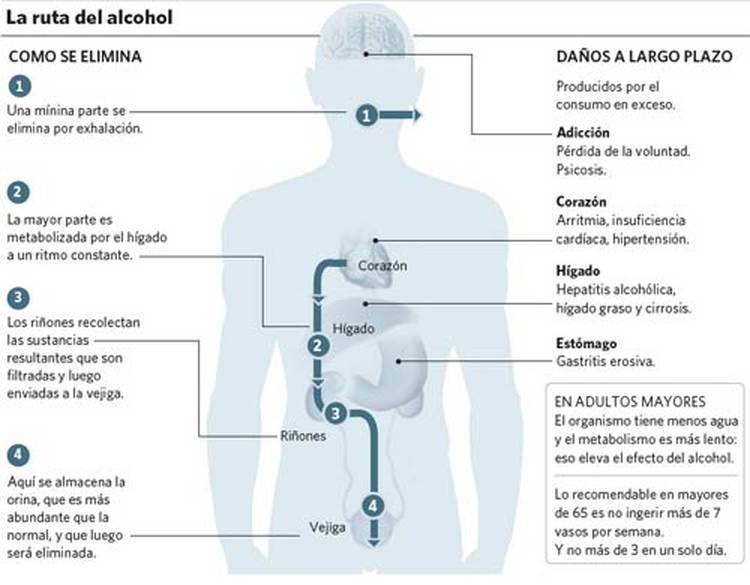

Cuando ingerimos el alcohol, este se convierte de etanol a acetato en el hígado y posteriormente se libera a la sangre donde viaja a través del torrente sanguíneo a otros órganos, incluyendo el cerebro, para usarlo como sustrato energético y para participar en la biosítesis de colesterol.
¿Quieres descubrir paso a paso cómo te afectará esa copa de más? Pues muy atento:
Etapa 1: "Uno al año no hace daño": El alcohol llega a la sangre entre 30 y 60 minutos después de ser ingerido, cuando el intestino delgado hace la absorción y lo envía por el torrente sanguíneo a todos los tejidos del cuerpo.
Etapa 2: "Yo tolero muy bien el alcohol": Inicialmente, la persona refleja un estado de euforia, enrojecimiento de su rostro, pasando al desequilibrio, descoordinación. Para reflejar después debilidad y agotamiento físico debido a la disminución del azúcar en la sangre produciendo visión borrosa así como eliminación de líquido acelerado.
Etapa 3: "La cabeza me estalla": La rápida eliminación de líquido que ocasiona su consumo, hace que el riñón tenga que absorber agua de otros órganos y es por esa razón que ocasiona dolor de cabeza, seguido de agresividad y disminución de la capacidad a la hora de tomar decisiones.
Etapa 4: "Usted no sabe quién soy yo": El alcohol también ingresará al intercambio gaseoso en los pulmones, detectándolo en el aliento con el alcoholímetro y, generalmente, la medición es directamente proporcional a la concentración de alcohol en sangre.
Etapa 5: "No vuelvo a beber": Pasado este estado de embriaguez se entra en un nivel de intoxicación etílica determinado por los siguientes signos:
¿Quieres descubrir paso a paso cómo te afectará esa copa de más? Pues muy atento:
Etapa 1: "Uno al año no hace daño": El alcohol llega a la sangre entre 30 y 60 minutos después de ser ingerido, cuando el intestino delgado hace la absorción y lo envía por el torrente sanguíneo a todos los tejidos del cuerpo.
Etapa 2: "Yo tolero muy bien el alcohol": Inicialmente, la persona refleja un estado de euforia, enrojecimiento de su rostro, pasando al desequilibrio, descoordinación. Para reflejar después debilidad y agotamiento físico debido a la disminución del azúcar en la sangre produciendo visión borrosa así como eliminación de líquido acelerado.
Etapa 3: "La cabeza me estalla": La rápida eliminación de líquido que ocasiona su consumo, hace que el riñón tenga que absorber agua de otros órganos y es por esa razón que ocasiona dolor de cabeza, seguido de agresividad y disminución de la capacidad a la hora de tomar decisiones.
Etapa 4: "Usted no sabe quién soy yo": El alcohol también ingresará al intercambio gaseoso en los pulmones, detectándolo en el aliento con el alcoholímetro y, generalmente, la medición es directamente proporcional a la concentración de alcohol en sangre.
Etapa 5: "No vuelvo a beber": Pasado este estado de embriaguez se entra en un nivel de intoxicación etílica determinado por los siguientes signos:
- Debilita el sistema nervioso central, incluso acciones involuntarias como el reflejo faríngeo y la respiración pueden disminuir o detenerse.
- Pupilas dilatadas.
- Aumenta el peligro de ahogarse con el propio vómito.
- Ocasiona hipotermia (temperatura extremadamente baja).
- Provoca que el nivel de glucosa en sangre baje extremadamente, lo que puede producir convulsiones, daño cerebral y muerte.
- Induce un ritmo cardíaco irregular, pueden ser latidos cardíacos rápidos o que el corazón deje de latir.
- Lleva a la pérdida de conciencia.
- Produce problemas en el aparato digestivo, como dolor abdominal, gastritis o sangrado intestinal.
- Origina alteraciones del funcionamiento general del hígado.
miércoles, 9 de agosto de 2017
Usos de los elementos de la tabla periódica.
Todavía me acuerdo de los primero días enfrentándome a la tan temida Tabla Periódica.
Ahora nos plantemos cual es la mejor forma de aprenderla, de entenderla, de saber todas esas sorpresas que nos tiene guardada en su interior. Pues bien, indagando un poco estos días hemos visto en las noticias que un diseñador ha creado una tabla con ilustraciones de todos los posibles usos de los diferentes elementos.
¿Nunca te has planteado por ejemplo para qué se utiliza el estroncio (Sr)? Pues si te fijas en la tabla verás que se utiliza para la fabricación de fuegos artificiales.
Sin duda alguna cosas así deben de ser compartidas para facilitar un poquito más aún si cabe la tediosa labor de conocer algo más sobre la Tabla Periódica.
Su idea puede ser descargada en PDF aquí mismo:
viernes, 2 de diciembre de 2016
Estamos de estreno: Cuatro nuevos elementos en la Tabla Periódica
Si, habéis leído bien, ¡estamos de estreno con 4 nuevos elementos en la tabla periódica!
Este avance, de gran valor científico, ha sido anunciado por la propia IUPAC a tráves de su cuenta de Twitter:
La IUPAC (Unión Internacional de Química Aplicada y Pura), un organismo formado por representantes de las sociedades nacionales de química de todo el mundo, ha aprobado los nombres de los cuatro nuevos elementos que, desde principio de este año eran candidatos a engrosar la tabla periódica. Ya lo pudísteis leer en el anterior post Nihomio, moscovio, tenesino y organesón nuevos nombres para la tabla periódica.
Pero ya es oficial, después de este Jueves la última fila de la Tabla Periódica de los elementos que ha traído de cabeza a más de un estudiante, cuenta con cuatro nuevas incorporaciones cuyas nomenclaturas y símbolos químicos ya son oficiales.
Los nuevos cuatro inquilinos de esta tabla de elementos químicos, naturales y artificiales, disponibles en la naturaleza, fueron probados inicialmente en pequeñas cantidades en aceleradores de partículas y encierran información importante para entender cómo funcionan los núcleos atómicos.
Este avance, de gran valor científico, ha sido anunciado por la propia IUPAC a tráves de su cuenta de Twitter:
En concreto, se han incorporado a la tabla los elementos 113, 115 y 118. Todos ellos muy pesados, con un alto número atómico y alta presencia de protones en sus núcleos.
También ha validado sus nombres que ya son Nihonio, Moscovio, Téneos y Oganesón.
miércoles, 2 de noviembre de 2016
La importancia del cambio de unidades.
Todos los que hemos estudiado ciencias, estamos hartos de escuchar frases tan típicas y repetitivas como estas:
* Fijaos en las unidades.
* Comprobad que son consistentes.
* Comprobad que le habéis puesto unidades al resultado.
* Comprobad que las unidades del resultado final son las que deben ser.
* Comprobad si hay que hacer cambios de unidades en los datos iniciales del problema antes de operar...
Tras años metiendo la pata, ahora, que somos nosotros los que damos las clases, también torpedeamos las cabezas con estas frases. Y esque no me cabe duda de que a muchos alumnos les suena a mero sermón de profesor pesado y "bufan" cada vez que lo oyen.
Otros, preguntan que para qué sirve esto. ¿De qué sirve todo este rollo de cambiar de unidades?...
Pues sinceramente, hubiese estado genial que se lo hubiesen repetido un poquito más a los genios de la NASA que se encargaron de la Mars Climate. Porque a ellos sí que les hacía mucha falta, y, a la hora de la verdad, cuando los cambios de unidades no eran un mero aprendizaje académico sino que se la estaban jugando a una carga, fallaron estrepitosamente.
Os preguntaréis qué era Mars Climate. Pues bien, era una sonda espacial enviada para estudiar la temperatura, el nivel de CO2 de Marte. Esta sonda se mandó en Diciembre de 1998 y llegó a Marte en Septiembre de 1999.
Estáis pensando bien, el satélite de 193 millones de dólares, por no hablar de todo el trabajo, el tiempo y el esfuerzo, se fue a la basura. La Mars Climate se estrelló por causa de un error matemático de cambio de unidades.
Nunca llegó a orbitar en torno al planeta rojo ya que se acercó muchísimo más de lo previsto, dejando atrás la órbita calculada y destruyéndose por fricción con la atmósfera del planeta. Tenía que haberse acercado a unos 150 km y se acercó 100 km más, hasta los 50 aproximadamente. ¿Donde estuvo el error? Pues probablemente fuera el error más bochornoso de toda la historia de la NASA ya que el sistema de control en la Tierra y el de la nave no trabajaban en las mismas unidades. Mientras que uno trabajaba con el sistema anglosajón de unidades (más habitual en EEUU), el otro trabajaba en el sistema métrico decimal.
Así que ya sabéis, si alguna vez un alumno o un compañero de clase se queja de que somos pesados con las unidades y que esto no sirve para nada... recordadle que la Mars Climate nunca llegó a orbitar en torno a Marte y que 193 millones de dólares flotan ahora por el espacio a modo de chatarra espacial.
¿Quien dijo que el cambio de unidades no era algo crucial?

Etiquetas:
1º Bach,
2º Bach,
2º ESO,
3º ESO,
4º ESO,
Blog,
Ciencia,
curiosidades,
Docente,
Educación,
Factores de Conversión,
Física
viernes, 2 de septiembre de 2016
¿De qué están hechas las medallas de las Olimpiadas?
Después de unos días de descanso, desconectada de todo lo referente a la química, he encontrado esta foto que da qué pensar un poquito.
¿Conoces de qué están formadas las medallas que han ganado los deportistas en estas pasadas Olimpiadas en Río de Janeiro?
Indagando un poco he podido comprobar que el Comité Olímpico especifica un pequeño criterio de composición de las medallas, incluyendo las de oro que deberán contener al menos un 92,5% de plata y deberán al menos contener un 6% de oro; pero permiten variaciones.
En el caso de Rio de Janeiro, la medalla de Bronce estaba formada por una aleación de Cobre (95%) y Zinc (5%). Normalmente el bronce está formado por Estaño, pero este año en los Juegos Olímpicos de Rio de Janeiro las han elaborado con Cobre y Zinc.
Las medallas de plata estaban formadas en un 100% por plata, eso sí, obtenida de recursos reciclados, como partes de vehículos, rayos x…
Y lo que más me ha sorprendido es la poquita cantidad de oro que contienen, tan sólo un 1,2 % siendo el resto plata! :O
Curiosidades que dan que pensar ¿no creéis?
domingo, 12 de junio de 2016
Nihomio, moscovio, tenesino y organesón nuevos nombres para la tabla periódica
Tenemos que prepararnos para sustituir las tablas periódicas a final de año, y esque los descubridores de los elementos 113, 115, 117 y 118 ya han propuesto sus nombres: nihonio (Nh), moscovio (Mc), tenesio (Ts) y oganesón (Og) respectivamente.
Ya está abierto el plazo de alegaciones que durará hasta noviembre cuando pasarán a denominarse así de forma oficial.
La IUPAC los ha presentado de forma oficial esta semana y recomienda su aceptación. A finales de año, por tanto es muy probable que haya cuatro nuevos nombres en la tabla periódica, los de los elementos que completan la fila 7, que hasta ahora se llamaban de forma provisional ununtrium, ununpentium, ununseptium y ununoctium.
Siguiendo la tradición, se pueden poner nombres relacionados con la mitología, minerales y propiedades del elemento, o como ocurre en este caso, términos geográficos o referidos a un científico. En este caso se ha optado por denominar tres elementos en honor a Japón, Moscú y Tennessee, y uno en honor a un científico Ruso.
Quedará esperar a noviembre que será cuando la IUPAC confirme los nombres definitivos en inglés para posteriormente la RAE hará lo propio con los nombres en castellano.
jueves, 9 de junio de 2016
Como estudiar la tabla periódica
Eso debió de pensar Kanchi Chopra, una estudiante de ciencias en Delhi que ha ideado una manera genial para aprender la tabla periódica. Para amenizar el estudio, la joven ha relacionado cada uno de los elementos con un problema que afecta a la sociedad actual, como el fraude o el calentamiento global.
En esta tabla tan peculiar podemos ver representado por ejemplo al Francio (Fr), relacionado con el fraude, la C del Carbono relacionado con el cambio climático, el alzeimer con el Alumnio (Al)… Cuanto menos curioso para tenerlo en cuenta :D ...
jueves, 2 de junio de 2016
Periodic vídeos: Un vídeo para cada elemento de la tabla periódica
A veces resulta un rollo ponerse a estudiar la tabla periódica de memoria, pero no son pocas la opciones que hay para que resulte más ameno. Una de ellas es Periodic Videos, una tabla periódica digital donde cada elemento químico está ilustrado con un vídeo.
Está desarrollado por un equipo de químicos de la Universidad de Nottingham con ayuda de Brady Haran, realizador especializado en videojuegos divulgativos y la plataforma TEDEd. La tabla ofrece un montón de vídeos destinados a explicar las características, las propiedades y las aplicaciones de cada elemento.
Periodic Videos es una web de acceso gratuito, aunque sus vídeos pueden consultarse también desde la página de la Universidad de Nottingham o desde su canal en YouTube, el acceso desde el conocido entorno educativo ofrece al usuario más ventajas.
Los vídeos están en ingles en su mayoría con subtítulos, y su estilo cercano y desenfadado facilita la comprensión de la información.
Un ejemplo es el vídeo en el que experimenta con una hamburguesa de queso, dejándola a remojo unas 3 horas en ácido clorhídrico simulando nuestro proceso digestivo.
viernes, 13 de mayo de 2016
Ácidos y Bases
Hoy os propongo que visitéis el siguiente recurso sobre "reacciones de ácido y base".
Al finalizar la presentación, encontrarás un test para revisar lo aprendido y un breve resumen del tema. Además comentaremos alguna reacción entre ácidos y bases que ocurra en nuestro día a día.
lunes, 21 de marzo de 2016
Una clase diferente con Kahoot
Algunos de vosotros ya lo conoceréis pero este post va destinado tanto a profesores, para darlo a conocer, como a alumnos para que aprendan a utilizarlo. Muchos os preguntaréis de qué se trata, pues es una de esas aplicaciones que pueden llegar a ser de gran ayuda en el cambio de metodologías en el aula.
Se trata de Kahoot, un sistema de respuesta basado en el juego, con el que se obtiene feedback de nuestro alumnos en tiempo real. Nadie mejor que sus creadores para describirla:
Kahoot es una plataforma de aprendizaje mixto basado en el juego, permitiendo a los educadores y estudiantes investigar, crear, colaborar y compartir conocimientos. Se ofrece a los estudiantes una voz en el aula, y permite a los educadores que se dediquen y centren sus estudiantes a través del juego y la creatividad. Kahoot instiga experiencias como ésta y trabaja a través de dispositivos móviles. Sin embargo, hay un elemento social. Estamos alentando el intercambio (y colaboración) de grandes concursos, debates y encuestas. Nuestra filosofía y la visión es que la gente de todo el mundo deben compartir su contenido educativo para que otros jueguen en las aulas de todo el mundo. Este intercambio debe ocurrir dentro del mismo Kahoot o en las redes sociales como Facebook, Twitter y Pinterest. Internet permite esta colaboración, y la alentamos activamente.
En el siguiente vídeo puedes ver cómo comenzar este aventura:
Kahoot es por tanto un sistema de respuesta con el cual se pueden crear cuestionarios, encuestas y discusiones. Pero los creadores no solo han pensado en la pedagogía unidireccional en la que el docente cree preguntas y los alumnos se limiten a contestar en tiempo real, compitiendo entre sí (de ahí el aprendizaje basado en el juego), sino que buscan una pedagogía más activa por parte del alumnado.
jueves, 17 de marzo de 2016
8 curiosidades sorprendentes de la física que seguro que no conoces
- La gravedad y el paso del tiempo: La velocidad y la gravedad tienen un gran efecto en la forma en la que se percibe el tiempo, por lo que los astronautas en la Estación Espacial Internacional, quienes están bajo un cambio significativo en la gravedad comparada con la de la Tierra, experimentan el tiempo de forma más lenta, haciéndolos 1 segundo más jóvenes cada 747 días.
- La velocidad de la luz: Siempre que nos referimos a la luz la conceptualizamos como aquello que se mueve más rápido que todo lo demás, a una velocidad de 299792.458 km por segundo, pero esta velocidad es la de la luz en el vacío, siendo realmente que la luz modifica su velocidad al atravesar diferentes medios. Incluso, existen experimentos en donde se ha metido una velocidad de 17 metros por segundo en el cero absoluto (-273.15ºC).
- La humanidad cabe en un terrón de azúcar: Seguramente has escuchado el concepto del espacio existente entre los átomos y cómo estos son prácticamente un espacio vacío entre el núcleo y los electrones. Si quitáramos todo el espacio vacío entre los átomos de toda la humanidad, quedaríamos como un pequeño terrón de azúcar, el cual pesaría cinco mil millones de toneladas y sería extremadamente denso.
- De qué está hecho el Universo: A pesar de los grandes avances en la astrofísica en las últimas décadas, más preguntas han surgido acerca de la composición del universo. Sabemos que la cantidad de materia visible (planetas, estrellas, objetos estelares) juntan el 2 % de la materia del universo, pero el resto está formado por lo que llamamos materia oscura y energía oscura, la cual aún no entendemos a fondo.
- Somos bombas de hidrógeno: La Ley de la conservación de la energía nos dice que toda la energía que se deposita en un sistema debe salir de alguna forma, es decir, esta energía no se puede destruir. En nuestros cuerpos depositamos una gran cantidad de energía, la cual queda almacenada con una cantidad de 7x10^18 Julios, si se liberara en un instante, tendría el poder de 30 bombas de hidrógeno.
- La teoría de los multiversos: Esta teoría es de las más controvertidas, y explica que existe una cantidad infinita de universos cada uno con unas cuantas diferencias entre ellos. Todo lo que imaginas está pasando en otro universo, incluso tu inmortalidad y tu misma muerta. En un universo morirás al levantarte de tu silla, en otro ya lo hiciste a causa de un infarto y en otro tu muerte pasará dentro de millones de años, de ahí la teoría de la inmortalidad cuántica.
- La gran implosión: La conocida teoría del Big Bang es la más aceptada en la actualidad respecto a la creación del Universo que conocemos. Pero esta misma teoría dio origen a la teoría de la Gran Implosión, la cual menciona que el universo no sólo disminuirá su velocidad de expansión, sino que también se regresará todo en una implosión. No se sabe si esto de verdad pasará; pero la teoría describe que de ocurrir así, ha pasado antes y este no es el primer universo en experimentarlo.
- La relación entre masa, energía y velocidad: La famosa ecuación E=mc^2 nos explica cómo la masa y la energía son parte de lo mismo por lo que si mueves un objeto le estás agregando energía y, por lo tanto, masa. El incremento de masa es imperceptible a velocidades cotidianas, pero mientras te acercas a la velocidad de la luz, la energía que se debe depositar en el objeto es enorme, por lo que la masa aumenta de forma considerable, pero este incremento es sólo temporal, por eso un avión no llega más pesado a su destino.
Fuente: Curiosidades Batanga
lunes, 14 de marzo de 2016
14 de Marzo: Día de Pí
¿Sabes que hoy se celebra en todo el mundo el día de Pi? 3,1415926535897932384…Se trata del número Pi, una cifra infinita que indica la constante proporción de una circunferencia con su diámetro. Normalmente nosotros lo reducimos a 3,14 en su expresión más simple, y se representa con la letra griega.
En 2009 la Cámara de Representantes de los EEUU declaró la celebración del Día de Pi el 14 de marzo, después de que el físico Larry Shaw lo propusiera y fuera ganando popularidad.
El número Pi es una de las constantes matemáticas más importantes, también vital en otras ciencias y áreas del conocimiento. Muchos proyectos no se podrían levar a cabo, o sería muy difícil sin el número Pi (como la arquitectura, ingeniería o mecánica), ya que sirve para calcular diferentes longitudes y espacios.
Y os preguntaréis por qué se celebra hoy el día de Pí. Pues por la forma en que se escribe en el formato usado en los Estados Unidos, el 14 de marzo (3/14). Habitualmente, la celebración se concentra a las 01:59 PM (en reconocimiento de la aproximación de seis dígitos: 3,14159).
Matemáticos y profesores de varias escuelas del mundo, organizan fiestas y reuniones en esa fecha. La fecha se celebra de maneras muy diversas: algunos grupos se reúnen para discutir y comentar sobre la importancia de pi en sus vidas, intercambiar anécdotas o teorizar cómo sería el mundo sin el conocimiento de pi. Otros grupos se reúnen para ver la película de culto "Pi, fe en el caos", y también es frecuente comer tartas con motivos sobre Pi, otro juego de palabras, ya que en la lengua ingles, tanto pi como pie (tarta) tienen idéntica pronunciación.
¿Te animas a celebrar el día de Pí?
viernes, 11 de marzo de 2016
Tabla periódica dinámica
En el siguiente enlace puedes encontrar una tabla periódica dinámica que te ayudará para estudiarla y conocer las propiedades más importantes de todos los elementos. ¿A que así resulta mucho más fácil?
Suscribirse a:
Entradas (Atom)





























